Симптомы дистрофии у детей
Клиническая картина имеет особенности в зависимости от формы и степени тяжести заболевания.
При лёгкой форме гипотрофии
I степень отклонения от нормы можно выявить лишь при тщательном исследовании. В данном случае общее состояние ребёнка никак не страдает. Возможны следующие патологические изменения: снижение тургора (эластичности) кожи, истончение подкожно-жирового слоя на передней брюшной стенке.
Среднетяжёлая форма гипотрофии
II степень характеризуется вялостью и апатичностью ребёнка, ухудшением аппетита, незначительным отставанием в умственном развитии. Также наблюдается уменьшение тургора и сухость кожи, снижение мышечного тонуса и общей температуры тела. Нормальное количество подкожной жировой клетчатки остаётся лишь на лице, на других же участках тела она значительно истончена. Кроме того, возможно увеличение частоты дыхания и сердцебиения, нарушение стула. При данной форме нередко возникают сопутствующие заболевания (гаймориты, пневмонии, пиелонефрит и др.).
Тяжёлая форма гипотрофии

III степень проявляется сонливостью, повышенной возбудимостью и раздражительностью, отставанием в физическом и психическом развитии. Визуально отмечается бледность кожи, отсутствие на всех участках тела подкожной жировой клетчатки, «свисание» кожных складок и «старческое» лицо. Выявляются также мышечная атрофия на фоне повышенного тонуса, высыхание слизистых оболочек и роговицы, полная утрата тургора кожи. Значительно снижается температура тела, возникает недостаточность сердечно-сосудистой и дыхательной системы, дисфункция желудочно-кишечного тракта.
При гипостатуре наблюдается равномерное отставание в массе тела и росте ребёнка. Единственное отличие в том, что кожа и подкожно-жировой слой не подвергаются выраженным изменениям. Она, как правило, возникает вторично на фоне хронических заболеваний. Её развитие также нередко связано с определёнными переходными периодами развития ребёнка. Одним из таких периодов является первое полугодие жизни малыша, когда вводится докорм. Появление на втором году жизни данной патологии, прежде всего, связано с врождёнными хроническими заболеваниями. Таким образом, устранение причины приводит к постепенной нормализации роста.
Алиментарный маразм. Такое истощение, как правило, встречается у детей школьного возраста. При этом отмечается недостаток белков и калорий.
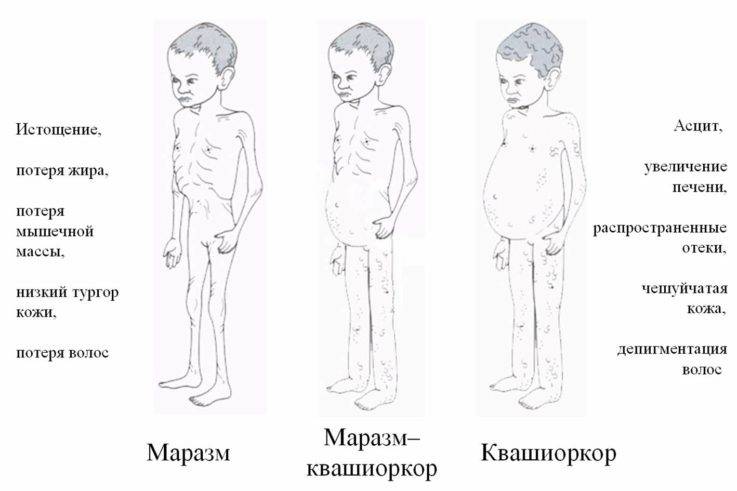
К основным и постоянным симптомам относят:
- дефицит массы тела достигает 60% от возрастной нормы;
- истощение подкожно-жирового слоя;
- уменьшение мышечной массы;
- кожа обтягивает все кости, на лице появляются морщины, и оно похоже на лицо старика;
- конечности становятся очень тонкими.
Кроме того, отмечается ряд патологических нарушений, вызванных белково-калорийной недостаточностью: ухудшение памяти, снижение работоспособности и умственно-познавательных способностей, падение остроты зрения, особенно в сумеречное время, повышенная ломкость кровеносных сосудов, в результате чего можно заметить на коже мелкоточечные кровоизлияния даже после лёгкого щипка.
Паратрофия зачастую развивается вследствие нерационального питания ребёнка. При этом отмечается умеренная адинамия и снижение тонуса мышц. Возможно беспричинное беспокойство. Дети старшего возраста жалуются на головные боли, одышку и повышенную утомляемость. Аппетит чаще всего снижен. Кожа бледная, подкожный жировой слой чрезмерно развит (особенно в области передней брюшной стенки и бёдер), однако, тургор кожи снижен. Часто при паратрофии наблюдается диспропорциональное телосложение.
Основы комплексного лечения
Лечить детскую дистрофию нужно только после консультации врача. В зависимости от степени заболевания он подберет наиболее щадящее и эффективное лечение и составит специализированный рацион для ребенка.
Правила питания
При данном заболевании делается уклон на так называемую «омолаживающую» диету. Ребенка нужно кормить несколько чаще и, возможно, немного большими порциями
. Объем и энергетическую ценность питания для маленького пациента должен рассчитать врач. При расчете необходимо полагаться на общую массу тела малыша. Зачастую энергетическая ценность пищи для кормления должна на 20% превышать норму.
Отдельно рассчитывается уровень жиров, углеводов и белков в рационе. Жиры по возможности вообще исключают, так как при дистрофии в организме ребенка вырабатывается недостаточно ферментов для их расщепления. Углеводы остаются на уровне нормы, а вот белковой пищи нужно употреблять немного больше нормальных показателей. Соотношение жиров, углеводов и белков в детском рационе при дистрофии должно быть таким: 1:3:6.
Знаете ли вы?
Ген д
истрофина отвечает за возникновение наследственной дистрофии человека.
Изменение качественного состава рациона производится постепенно, при этом проводится контроль усвоения питательных веществ организмом ребенка. Рекомендуется раннее добавление в рацион желтков и овощных либо фруктовых пюре. При всем этом необходимо точно рассчитать нормы витаминов и , потребляемых малышом за сутки.

В случае полигиповитаминоза необходимо резко увеличить количество недостающих витаминов в рационе. Но помните: всем этим должен заниматься лишь опытный врач, который составит оптимальный рацион после проведения тщательной диагностики.
Медикаментозное лечение
Медикаментозная терапия будет назначена педиатром лишь в том случае, когда есть острая необходимость нормализировать состояние здоровья ребенка и не допустить различных осложнений. При медикаментозной терапии зачастую используется следующее:
- Терапия с пероральным вводом некоторых пищевых ферментов. В большинстве случаев назначается с первых дней лечения дистрофии. Такое лечение подразумевает употребление следующих препаратов: соляная кислота с пепсином и панкреатин с углекислым кальцием.
- Терапия витамином С и витаминными соединениями из группы В (дозы должны в 3-5 раз превышать норму). Витамин А и вводят лишь в случае выявления их дефицита в организме малыша.
- терапия используется для устранения проблем с метаболизмом. В данном случае могут быть назначены следующие препараты: «Инсулин», «Префизон», «Неробол», «Ретаболил», «Тиреоидин».
- Терапия для общей стимуляции организма подразумевает следующее: введение донорской крови и у-глобулина, использование ректальных свеч «Апилак».
- Врожденная дистрофия часто поражает ЦНС. В таких случаях для предотвращения сильных осложнений могут применяться «Церебролизин» и глутаминовая кислота.

Важно!
Дистрофия в детском возрасте может возникнуть из-за формирования камней в желчном пузыре.
Следует понимать, что лечение дистрофии — сложный и длительный процесс. Все это время родители должны тщательно следить и ухаживать за ребенком. Правильное питание и соблюдение всех указаний педиатра — первый шаг на пути к исцелению.
Стадии дистрофии
В протекании алиментарной дистрофии выделяют три стадии.
- Масса тела снижена незначительно, работоспособность в целом сохранена. Пациенты предъявляют жалобы на слабость, зябкость, повышенный аппетит, жажду и учащенное мочеиспускание.
- Отмечается значительное похудение и снижение работоспособности. Пациенты не могут выполнять свои профессиональные обязанности, но способность к самообслуживанию сохранена. Уровень белка в крови значительно снижен, что приводит к появлению безбелковых отеков. Периодически возникают эпизоды гипогликемии ;
- Пациенты резко истощены, не способны самостоятельно передвигаться. Может развиться голодная кома.
Клиническая картина алиментарной дистрофии нарастает медленно, и на протяжении долгого времени пациенты не чувствуют себя больными. Первые признаки заболевания обычно остаются незамеченными. К ним относятся:
- повышенный аппетит и жажда;
- постоянная сонливость;
- снижение работоспособности;
- раздражительность;
- слабость;
- полиурия.
Одним из первых специфических симптомов дистрофии является повышенная потребность пациентов в соленой пище, вплоть до поедания чистой поваренной соли.
При дальнейшем прогрессировании алиментарной дистрофии кожные покровы утрачивают свою эластичность, становятся сухими и дряблыми, повисают выраженными складками и своим видом напоминают лист пергамента.
Значительно страдает общее состояние пациентов. Становится тяжело выполнять любую физическую работу. Затем появляются признаки дистрофического поражения внутренних органов:
- диспепсические проявления (запоры , метеоризм , отрыжка);
- снижение температуры тела;
- стойкое понижение артериального давления;
- снижение либидо;
- прекращение менструальной функции;
- бесплодие;
- расстройства психики.
На последней стадии алиментарной дистрофии начинают угасать все функции организма больного. Мышцы истончаются и становятся дряблыми. Подкожный жировой слой полностью исчезает. Пациент теряет способность передвигаться самостоятельно.
Нарушения минерального обмена приводят к повышенной ломкости костей, возникновению переломов даже под влиянием минимальных физических нагрузок. Угнетаются процессы кроветворения, в крови снижается содержание лейкоцитов, эритроцитов, тромбоцитов. Накопление продуктов катаболизма в крови оказывает негативное воздействие на центральную нервную систему, что становится причиной стойких расстройств психики.
Формы
По характеру клинического течения миопатию разделяют на 2 формы:
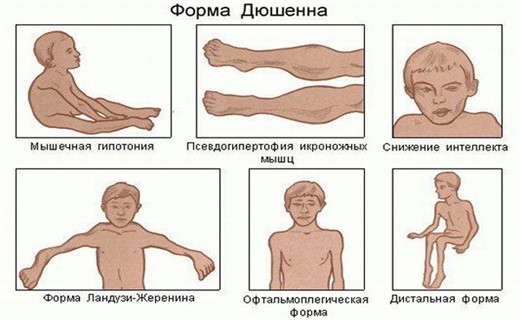
Мышечная дистрофия Дюшенна — начальный этап развития болезни, который характеризуется маловыраженными проявлениями. У многих детей уже на первом году жизни отмечается дебют мышечной миопатии Дюшенна. Родители замечают отставание моторного развития, при котором малыши начинают сидеть, вставать и ходить позже сверстников. По мере развития дистрофии у детей к 5 годам наблюдается мышечная слабость, астения при ходьбе, походка с переваливанием туловища с боку на бок, а также симптом Говерса (ребенок не может встать без помощи рук).
Прогрессирующая дистрофия Дюшенна — отличается выраженной клинической картиной. К 8-10 годам мышечная слабость приводит к существенным ограничениям физических возможностей и активности. В подростковом возрасте дети с данной формой миопатии Дюшенна передвигаются с помощью инвалидного кресла. Кроме того обширный дистрофический процесс приводит к быстрому снижению жизненной емкости легких и проблемам с дыханием.
Симптомы и признаки
Миопатия Дюшенна сопровождается следующими симптомами:
- Поражение скелетных мышц. При данном заболевании мышечная атрофия стремительно распространяется на мускулатуру спины, плечевой пояс и проксимальные области рук. В результате, у детей сильно выпирают лопатки, формируется непропорционально тонкая талия. Типичные признаки дистрофии Дюшенна — псевдогипертрофия мышц голени и арефлексия, при которой выпадают сухожильные рефлексы коленей, а также плечевого бицепса и трицепса. При этом долгое время могут сохраняться рефлексы икроножных мышц и лучевой кости.
- Деформации скелета. Мышечная дистрофия Дюшенна приводит к серьезным деформациям костно-суставной системы. У детей нарушается правильная конфигурация позвоночного столба, развивается сколиоз, лордоз или кифоз, деформируются стопы, грудная клетка приобретает седловидную или килевидную форму.
- Поражение сердечной мышцы. Прогрессирование дистрофии Дюшенна затрагивает сердечные мышцы, поэтому у трети детей в возрасте 13-14 лет развиваются сердечно-сосудистые расстройства: дилатационная кардиомиопатия, аритмия, неустойчивость артериального давления. После 18-20 лет поражение сердечной мышцы протекает бессимптомно, поскольку в этот период пациенты уже не могут осуществлять двигательную активность.
- Умственные нарушения. В 30 % случаев при дистрофии Дюшенна наблюдается снижение интеллектуальных способностей различной степени выраженности. При этом нарушения не соотносятся с тяжестью самой болезни или объемом поражений скелетных мышц. В основном у детей преобладают расстройства слуховой памяти, дефекты речи, трудности с концентрацией внимания. Нередко присутствуют симптомы олигофрении, аутизма, дислексии.
- Эндокринные расстройства. Более чем у половины детей и подростков с дистрофией Дюшенна нарушается нормальное функционирование желез внутренней секреции, что сопровождается нейроэндокринными расстройствами: синдромом Иценко-Кушинга, адипозогенитальной дистрофией.
Чтобы получить более подробную информацию или консультацию специалиста по орфанным заболеваниям, заполните все поля формы. Наши консультанты будут рады Вам помочь.
Профилактика
Пренатальная профилактика, направленная на предупреждение развития внутриутробной дистрофии, включает в себя: полноценный сон, режим работы и отдыха, сбалансированное питание, посильные физические упражнения, контроль веса женщины, регулярный мониторинг состояния здоровья женщины и плода. Постнатальная профилактика дистрофии у ребёнка наилучшим образом осуществляется при естественном вскармливании, постоянном контроле над ежемесячными прибавлениями роста-веса в течение первого года и ежегодном мониторинге дальнейшей динамики физического развития. Предупреждение дистрофии у взрослых пациентов возможно при условии достаточного питания, заместительной терапии энзимопатии и мальабсорбции, а также лечения основных иммунодефицитных состояний.
– это заболевание, характеризующееся тяжелой белковой и чаще более выраженной энергетической недостаточностью. Проявления могут быть самыми различными, основные — потеря массы тела более 20% (или ИМТ менее 16), сухость и дряблость кожи, ломкость волос и ногтей, вялость, сонливость и слабость, повышенный аппетит. Диагностика строится в основном на анамнезе, сочетании объективных и субъективных признаков, а также на исключении других заболеваний. Лечение комплексное, заключается в налаживании питания и восстановлении запасов питательных веществ, витаминов и микроэлементов в организме.
Следует заметить, что развитие дистрофии возможно только при длительном энергетическом голодании. При этом в организме сначала полностью истощаются запасы гликогена и жиров, затем для обеспечения основного обмена используются запасы внутритканевого белка. В первую очередь процессы дистрофии начинаются в коже, мышцах, затем задействуются внутренние органы, в самую последнюю очередь – жизненно важные (сердце, почки и мозг). В какой-то момент процессы катаболизма принимают такую форму, что летальный исход становится неизбежным даже при начале полноценного лечения.
На последних стадиях заболевания в организме истощаются запасы витаминов и минералов, перестает функционировать иммунная система. Летальный исход обычно наступает или от сердечной недостаточности , или от присоединившейся инфекции на фоне значительного угнетения иммунитета.
Общая информация
Изучая разнообразные виды дистрофии (смешанные, жировые, сосудистые, мышечные и прочие), врачи выявили несколько механизмов, провоцирующих патологические процессы. Генетическими сбоями, нюансами состояния организма в период эмбрионального развития или уже после рождения может объясняться клеточная энзимопатия: определенные метаболиты производятся слишком много или мало либо процессы их синтезирования сбиваются, что приводит к дисметаболизму. Дистрофия возможна по причине изменения обменных процессов на клеточном уровне, сбоя химических реакций, а также нарушения структуры клеточных мембран, ядер. Возможно нарушение субклеточных структур, сопровождающееся деструкцией комплексов, клеток.
Некоторые виды дистрофии объясняются инфильтрацией, когда из пространства между тканями в клетку в избыточном объеме поступают жидкости. Свою роль может сыграть эндоцитоз, то есть слишком активные процессы всасывания клеткой веществ. Дистрофия возможна на фоне снижения количества питательных компонентов, поступающих извне. Нередки случаи совмещения нескольких причин сразу.
Лечение дистрофии сетчатки
Своевременно начатое лечение дистрофии сетчатки помогает улучшить остроту зрения, остановить прогрессирование патологических изменений в тканях глаза и предотвратить появление грозных осложнений.
Для лечения дистрофий сетчатки применяют комплексный подход. Ввиду того, что большинство случаев заболевания носит наследственный характер, лечение болезни их симптоматическое, направленное на поддержание достаточной остроты зрения.
Медикаментозное лечение включает применение лекарственных препаратов с различным механизмом действия, цель которого – улучшение питания тканей сетчатки. Обычно применяют сосудорасширяющие препараты (но-шпа, папаверин), дезагреганты (аспирин, клопидогрель), комплексные витаминные препараты, укрепляющие стенки сосудов сетчатки (аскорутин, препараты с лютеином), биогенные стимуляторы и пептиды (ретиналамин, экстракт алоэ). При обнаружении экссудативной формы ВМД показаны интравитреальные инъекции препаратов из группы блокаторов неоангиогенеза (anti-VEGF препараты), дексаметазона, рассасывающих препаратов (гепарин, этамзилат).
Физиотерапевтическое лечение при дистрофии сетчатки включает магнитотерапию, лазерную стимуляцию сетчатки, электрофорез с лекарственными препаратами, улучшающими питание тканей (но-шпа, никотиновая кислота и пр.).
Аппаратное лечение возможно и в домашних условиях — использование прибора АМВО-01, разработанного специально для применения у пациентов с патологией сетчатки и зрительного нерва.
Лазерная коагуляция при дистрофии сетчатки
Наиболее эффективным методом лечения у пациентов с дистрофиями сетчатки является лазерная коагуляция (фотокоагуляция) сетчатки. Цель такого лечения – отграничение измененных областей сетчатки от окружающих их здоровых тканей для предотвращения прогрессирования болезни и развития возможных осложнений. Местное воздействие лазерных лучей повышает температуру в области обработки и вызывает ограниченную коагуляцию тканей и образование прочных сращений между сетчаткой и прилежащей к ней сосудистой оболочкой.
Хирургическое лечение показано при выявлении грубых сращений (шварт) между сетчаткой и стекловидным телом глаза, а также неоваскулярных мембран. С этой целью применяют витреоретинальные операции (витрэктомия, склеропломбаж, экстрасклеральное пломбирование и пр.).
Диагностика
Постановка диагноза «дистрофия» осуществляется на основе характерных клинических признаков, включая соотношение массы тела к росту, оценку тургора тканей, количество и размещение подкожной жировой клетчатки, анализ сопротивляемости организма к инфекционным заболеваниям. Степень гипотрофии определяется по результатам лабораторных исследований крови и мочи. Гипотрофия первой степени — лабораторные исследования крови и желудочной секреции указывают на диспротеинемию, выраженную в дисбалансе фракций белков крови и сниженную активность пищеварительных ферментов.
Гипотрофия второй степени — по данным лабораторных исследований у пациентов с дистрофией на этой стадии ярко выраженная гипохромная анемия со сниженным количеством гемоглобина в крови. Также диагностируется гипопротеинемия с низким содержанием общего белка в крови на фоне значительного снижения ферментной активности. Гипотрофия третьей степени — лабораторные исследования указывают на сгущение крови с замедленной скоростью оседания эритроцитов и наличие в моче значительных количеств мочевины, фосфатов, хлоридов, иногда ацетона и кетоновых тел.
Дифференционный диагноз «гипостатура» устанавливается методом исключения заболеваний, сопровождающихся отставанием физического развития, например, гипофизарного нанизма, при котором гипофиз человека не вырабатывает достаточного количества соматотропных гормонов, или других мутационных типов нанизма с достаточной секрецией соматропина, но нечувствительностью к нему организма. Другими вариантами генетически обусловленной низкорослости могут быть различные формы дистрофий, выраженные в аномальных пропорциях скелета. Изучение семейного анамнеза позволяет дифференцировать паратрофию и гипостатуру от семейной конституциональной низкорослости.
Общие сведения
Алиментарная дистрофия (алиментарный маразм) — это социальное заболевание, которое может развиться в результате вынужденного или осознанного голодания. На сегодняшний день алиментарным маразмом страдают люди не только в развивающихся странах, во время войн и катастроф – а это более полумиллиона человек. Многие готовы морить себя голодом осознанно в погоне за красивой фигурой и в угоду своим комплексам. Однако заболевание может иметь тяжелые последствия, вплоть до летального исхода. При длительном голодании, отсутствии поступления незаменимых веществ в организме могут произойти необратимые изменения метаболических процессов. В развитых странах все чаще можно услышать о случаях анорексии — а это та же алиментарная дистрофия тяжелой степени.
Классификация и симптомы
На сегодняшний день существует много различных классификаций данной патологии. Классификация происходит в зависимости от типа дисфункций метаболизма, локализации и происхождения. Наиболее часто в современной медицинской практике дистрофию разделяют на следующие типы: невропатическая, нейродистрофическая, нейроэндокринная и энцефалопатическая.
Каждый из типов дистрофии у ребенка имеет определенные симптомы и признаки:
-
Невропатическая:
общая масса тела снижена не более чем на 10% от нормы, возникают проблемы со сном, нарушается аппетит, угнетается настроение, появляется раздражительность и чрезмерная вспыльчивость. -
Нейродистрофическая:
первичная анорексия, общая масса тела снижена более чем на 10%, отставание в психическом и умственном развитии. -
Нейроэндокринная:
врожденный дефицит массы тела (более чем на 20% от нормы), угнетение психического и физического развития, гемиасимметрия, микроторакоцефалия. -
Энцефалопатическая:
ярко выраженные дефекты психомоторного и физического развития, выраженная нехватка различных типов в организме, полное отсутствие аппетита, локальное повреждение мозговых участков, нарушения развития костной системы.
- регулярная тошнота и ;
- или (запоры приводят к отсутствию стула на протяжении 3-5 дней);
- проблемы с кожным покровом (сухость, бледность, шелушение верхних слоев эпидермиса);
- плаксивость, апатия;
- снижение уровня АД, нарушение сердечного ритма.
Важно!
При дистрофии у ребенка может наблюдаться пониженная температура тела (ниже 36,6°С).
 возможных последствийгенетической предрасположенностиконкретном случае
возможных последствийгенетической предрасположенностиконкретном случае
Происходит нарушение обмена белков, жиров и углеводов (чаще чего-то одного из трех), вследствие чего сильно повышается риск летального исхода еще в грудном возрасте.
Диагностика дистрофии в раннем детском возрасте подразумевает проведение сразу нескольких исследовательских процедур. Сначала педиатр проводит общий осмотр ребенка
, оценивает состояние его кожных покровов, тонуса мышц, осматривает малыша на равномерность распределения жировой клетчатки под кожей. Далее измеряется температура тела, исследуется сердечный ритм.
Очень много о состоянии малыша может рассказать общий и биохимический крови. Зачастую при разной степени и форме дистрофии в крови у ребенка выявляют снижение активности пищеварительных ферментов. Помимо этого может наблюдаться полигиповитаминоз, гипохромная , сгущения крови за счет и снижения скорости оседания эритроцитов.
Все эти факторы могут говорить о том, что ребенок страдает дистрофией. Для исследования внутренних органов (чтобы подтвердить или опровергнуть риск осложнений) могут применяться и рентгенография.
Профилактика врожденной и приобретенной дистрофии
Профилактика врожденной дистрофии подразумевает ведение правильного образа жизни будущей мамы. Основными правилами поведения являются:
- Беременная женщина должна избегать стрессовых ситуаций и повышенных физических нагрузок.
- Правильно и сбалансировано питаться, причем не только в «интересный» период, но и после родов (чтобы грудное молоко соответствовало всем нормам).
- Перед матери нужно избавиться от всех острых инфекционных заболеваний. Хронические болезни нужно регулярно поддерживать на оптимальном для здоровья уровне.
- Будущая мама должна отказаться от употребления алкоголя, наркотических веществ и табакокурения.
Знаете ли вы?
В 2014 году ученым удалось создать искусственную хромосому, которая позволит в будущем побороть врожденную мышечную дистрофию.
Для профилактики приобретенной формы болезни нужно следовать таким правилам:
- кормить ребенка грудью на протяжении установленного срока;
- правильно и своевременно ввести в детский рацион ;
- правильно подобрать тип молочной (для этого лучше проконсультироваться с педиатром);
- укреплять иммунитет ребенка всевозможными методами.
Теперь вы знаете, что такое дистрофия у детей и как ее вылечить
Но важно понимать, что данное заболевание отличается длительным курсом терапии, поэтому необходимо запастись терпением и внимательно следить за состоянием здоровья малыша
Дистрофия – нарушение трофики, т. е. питания, тканей и органов. Наиболее часто в практике сталкиваются с алиментарной дистрофией .
Алиментарная дистрофия – заболевание, развивающееся на фоне тяжелой белковой и энергетической недостаточности и проявляющееся значительной потерей массы тела (свыше 20%), ломкостью ногтей и волос, сухостью кожи, общей слабостью, вялостью, сонливостью, повышенным аппетитом.
Алиментарная дистрофия относится к группе социальных заболеваний и развивается в результате осознанного или вынужденного голодания. Более полумиллиона человек, проживающих в развивающихся странах, страдает от нее. Это заболевание регистрируется и во вполне благополучных странах – здесь к его возникновению приводит длительное соблюдение низкокалорийных диет в стремлении достичь «идеальной» фигуры.
При длительном голодании организм недополучает необходимые ему пластические вещества, что вызывает нарушения метаболических процессов. В результате у пациента развивается анорексия , по своей сути являющаяся алиментарной дистрофией.
Лечение дистрофии

В зависимости от формы и степени тяжести заболевания подбирается комплекс терапевтических мер. Если дистрофия имеет вторичный характер, лечится патология, ставшая ее причиной
При первичном развитии внимание уделяется коррекции питания с помощью диеты, которая сочетается с медикаментозным лечением, массажем, гимнастикой. Проводится санация хронических инфекций
Для гипотрофии 1 стадии госпитализация необязательна.
При критической потере массы тела, тяжелых формах лечение проводится в стационаре.
Больной изолируется в боксе, где поддерживаются оптимальная температура, влажность, обеспечивается защита от внешних раздражителей.
Диетотерапия
Цель метода – восстановление дефицита питательных веществ. Лечебное питание назначается с учетом порога толерантности больного к пище. Кормление проводится часто, маленькими дробными порциями (7–10 раз в день). Объем пищи постепенно увеличивается.
В дневнике питания записываются ее количество и качество, изменения стула, частота мочеиспускания.
Диета при дистрофии состоит из 3 этапов:
- Адаптационный. Восстанавливает функцию пищеварительной системы, позволяет вывести продукты распада, определить переносимость к пище. Для этого уменьшается ее суточная норма на 30–60%, в зависимости от стадии заболевания, в течение 2–7 дней. Пища принимается через каждые 2–3 часа.
- Репарационный. Переводит организм на нормальный режим питания. Объём пищи постепенно увеличивается, в состав включается необходимое количество белков, жиров, углеводов. Частота приема пищи уменьшается на 1–2 раза. Этап длится около 3 недель.
- Завершающий. Продолжается до восстановления пищеварительной функции, нормального веса. Частота трапезы сокращается еще на 1 раз, порции увеличиваются, калорийность продуктов повышается.
Медикаментозное лечение
Терапия лекарственными препаратами направлена на восстановление метаболических процессов:
- для усвояемости пищи назначаются ферменты Мезим, Фестал, Креон;
- внутривенно вводятся растворы белковых гидролизаторов – Альбумин или Левамин;
- назначаются курсы витаминов групп В и С, прием биологических добавок с микроэлементами, иммуностимуляторов;
- при тяжелых формах алиментарной дистрофии проводится переливание крови.
Диагностика дистрофии у детей
Диагноз и дифференциальная диагностика дистрофии
Диагноз дистрофии основывается на следующих клинических симптомах:
- снижение тургора тканей;
- последовательное исчезновение или уменьшение толщины подкожной жировой клетчатки на животе, конечностях, лице, а также избыточное и неравномерное ее отложение, отставание массы тела от его длины и других возрастных параметров;
- снижение порога толерантности к пище и сопротивляемости к инфекционным и другим воздействиям внешней среды.
Диагноз должен отражать вид дистрофии, время возникновения по отношению к моменту рождения; при наличии гипотрофии — ее степень и этиологическую принадлежность; периоды развития — начальный, прогрессирования, реконвалесценции.
- Дистрофию sui generis отличают от вторичных дистрофий, вызванных пороками развития желудочно-кишечного тракта и других органов, наследственной патологией, органическими и функциональными поражениями центральной нервной системы, эндокринными заболеваниями, о которых нужно думать во всех случаях тяжелой гипотрофии (II — III степени), не поддающейся лечению, а также паратрофии и ожирения, особенно сочетающихся со значительным отставанием психомоторного развития.
- Гипостатуру дифференцируют от заболеваний, сопровождающихся резким отставанием в физическом развитии, прежде всего нанизма, а также физиологического субнанизма, обусловленного особенностями семейного, национального или расового характера.
- Непропорциональный нанизм, вызванный ахондроплазией, врожденной ломкостью костей, тубулопатиями, отличается от гипостатуры грубой патологией скелета, которую невозможно объяснить сопутствующим дистрофии подостротекущим рахитом. Рентгенограммы костей и отклонения от нормы показателей фосфорно-кальциевого обмена позволяют исключить эти заболевания.
- Пропорциональный нанизм обусловлен поражением гипофиза или тяжелой врожденной патологией сердечно-сосудистой и дыхательной систем. Развивается обычно в более старшем возрасте и редко проявляется при рождении. Затруднения возникают при дифференциальной диагностике от примордиального (простого или первичного) нанизма, обусловленного нечувствительностью тканей организма к гормону роста. Низкие показатели массы и длины тела отмечаются уже при рождении. В дальнейшем прибавка в росте крайне незначительна. В крови увеличено содержание гормона роста. Отсутствуют клинические и лабораторные признаки дистрофии.
Причины
Во время беременности осложнение могут вызвать:
- Употребление спиртных напитков и курение;
- Несбалансированное питание;
- Инфекционные болезни;
- Гестоз или нарушения прикрепления плаценты;
- Возраст младше 18 и старше 40 лет ;
- Употребление наркотических веществ;
- Стресс, депрессия;
- Болезни центральной нервной системы.
Приобретенную форму болезни вызывают:
- Генетические заболевания – мегаколон, заячья губа, болезнь Гиршпрунга, волчья пасть;
- Синдром мальабсорбции;
- Панкреатит;
- Злокачественные опухоли в жкт;
- Холецистит (воспаление желчного пузыря);
- Неправильное питание ребенка;
- Недостаточное количество грудного молока.
Причины дистрофии у детей
Развитие врождённой дистрофии происходит под влиянием негативных факторов, нарушающих полноценное формирование и развитие плода:

- токсикозы беременных;
- возраст матери до 20 или старше 40 лет;
- отсутствие сбалансированного питания, курение и регулярные стрессы во время вынашивания ребёнка;
- работа будущей мамы на вредном производстве с повышенным уровнем шума, вибрациями, а также химическими веществами;
- болезни у беременной женщины (различные хронические инфекционные заболевания, патологии сердца и эндокринной системы);
- нарушения плацентарного кровообращения, патологическое прикрепление плаценты и другие отклонения в течение беременности.
Факторы, провоцирующие развитие приобретённой (постанатальной) дистрофии принято делить на внутренние и внешние.
К внутренним факторам относятся патологические состояния, в результате которых нарушается всасывание и переваривание пищи:
- хромосомные нарушения;
- различные отклонения в физическом развитии;
- патологии эндокринной или центральной нервной системы;
- синдром приобретённого иммунодефицита (СПИД);
- болезни желудочно-кишечного тракта;
- пищевая аллергия;
- наследственные заболевания: лактазная недостаточность (непереносимость белка, содержащегося в молоке и молочных продуктах), целиакия (нарушение усвоения белка, который содержится злаках), муковисцидоз (нарушенная работа внутренних органов, вырабатывающих слизь).
Группу внешних факторов развития дистрофии формируют те обстоятельства, в результате которых ребёнок не получает необходимого для формирования нормального веса объёма питательных веществ, а также которые тем или иным образом тормозят процессы переваривания и усвоения пищи.
1. Пищевой фактор является основной причиной данной формы дистрофии. В случае с маленькими детьми расстройство развивается из-за нехватки грудного молока, неправильного выбора смеси или позднего введения прикорма. У детей более старшего возраста её провоцирует несбалансированный рацион, а также недостаточное количество калорий, белков, жиров или углеводов.

2. Токсический фактор. К ним относятся пищевые интоксикации, неблагоприятное действие плохой экологии, длительный приём лекарств.
3. Социальный фактор
Недостаточное внимание со стороны взрослых или частые ссоры родителей провоцируют стресс и могут вызывать развитие дистрофии
Следует помнить о том, что основной причиной дистрофии у детей является неполноценное питание, которое приводит к недостаточному поступлению питательных веществ и энергии в организм, так называемая алиментарная дистрофия.































