СОДЕРЖАНИЕ
Гидроксид калия обычно продается в полупрозрачных гранулах, которые липнут к воздуху, поскольку KOH гигроскопичен. Поэтому конусы обычно содержат различное количество воды (как и карбонаты — см. ниже). Растворение в воде особенно заметно. Водные растворы различной концентрации иногда называют калиевой щелочью. Даже при высоких температурах твердый кон не легко обезвоживается. 11
Структура править
При более высоких температурах твердый KOH кристаллизуется в кристаллической структуре NaCl OH-группа является либо быстрой, либо случайной, поэтому OH-группа, по сути, представляет собой сферический анион размером 1,53 Å (между размерами Cl- и F-). При комнатной температуре группа OH упорядочивается, и среда вблизи центра K + деформируется, деформируясь с K + -. OH — 2,69-3,15 Å, в зависимости от ориентации группы OH. Кон образует ряд кристаллических гидратов, т.е. моногидрат Кона2 O, kon -2 h2 O и квадруплекс KOH-4H2 о 12
Термическая стабильность править
Как и Наох, Кох обладает высокой термической стабильностью на Обе стороны газообразного вида. Благодаря высокой стабильности и относительно низкой температуре плавления, его часто отливают в форме бусин или брусков с плавящейся, небольшой поверхностью и управляемыми свойствами.
Примеры решения задач
ПРИМЕР 1
| Задание | Вычислите массу гидроксида калия, который может прореагировать с концентрированным раствором соляной кислоты объемом 300 мл (массовая доля HCl 34%, плотность 1,168 кг/л). |
| Решение | Запишем уравнение реакции:
KOH + HCl = KCl + H 2 O. Найдем массу раствора соляной кислоты, а также массу растворенного вещества HCl в нем: m solution =V solution × ρ; m solution =0,3 × 1,168 = 0,3504 кг = 350,4г. ω = m solute / m solution × 100%; m solute = ω / 100% ×m solution ; m solute (HCl) = ω (HCl) / 100% ×m solution ; m solute (HCl) = 34 / 100% × 350,4= 11,91 г. Рассчитаем количество моль соляной кислоты (молярная масса равна 36,5 г/моль): n(HCl) = m (HCl) / M (HCl); n (HCl) = 11,91 / 36,5 = 0,34 моль. Согласно уравнению реакции n (HCl) :n (KOH) = 1: 1. Значит, n(KOH) = n(HCl) = 0,34моль. Тогда масса гидроксида калия, вступившего в реакцию будет равна (молярная масса — 56 г/моль): m (KOH) = n (KOH)× M (KOH); m (KOH) = 0,34× 56 = 19,04г. |
| Ответ | Масса гидроксида калия равна 19,04 г. |
Применение
Добавка Е 525 разрешена к применению во всех странах. Допустимая норма не установлена.
Пищевая индустрия использует гидроксид калия:

- для регулирования и стабилизации кислотности. Добавку включают в технологию производства шоколадных изделий, продуктов на основе какао;
- для обработки замороженных овощей (преимущественно картофеля). Едкий кали призван защитить от потемнения, укрепить волокна, сохранить цвет и товарный вид;
- для снятия кожицы и кожуры с фруктов, корнеплодов;
- в качестве катализатора при рафинации растительных масел (подсолнечного и льняного).
Добавка E 525 как регулятор кислотности разрешена в продуктах прикорма для детей от 12 месяцев.
Высокие моющие свойства вещества, способность стабилизировать уровень pH, улучшать текстуру продукта используют производители косметических средств и товаров бытовой химии. Добавку включают в состав отбеливателей, жидкого мыла, шампуней, лаков и красок для волос, средств для бритья, очистителей зубных протезов и многих других.
Стоматологи раствором едкого кали дезинфицируют зубные каналы.
Стабилизатор Е 525 нашел применение в различных промышленных сферах:

- выступает электролитом в щелочных элементах питания;
- эффективно очищает водопроводные и канализационные трубы от загрязнений;
- входит в систему очистки сточных вод;
- в составе инсектицидных препаратов уничтожает клопов, блох и других паразитов;
- в металлургии, химическом производстве нейтрализует отработанные вредные газы;
- свойство продукта снижать сопротивление грунта используют для создания очагов заземления электроприборов.
Гидроксид калия пользуется повышенным спросом в животноводстве и ветеринарии. Вещество обладает сильным антимикробным действием: убивает большинство вегетативных форм вирусов и споры бактерий.
Раствором едкого кали животным прижигают раны, очищают копыта, обрабатывают от паразитов. Вещество входит в состав пасты для удаления новообразований на коже лошадей, вызванных раком стрелки копыт.
Добавку E 525 используют для дезинфекции загонов, кормушек, вагонов для перевозки животных и других помещений и предметов.
Гидроксидом калия обеззараживают склады для хранения продуктов животноводства (мясо, молоко).
Сферы использования гидроксида калия
Это вещество известно своими очищающими свойствами с 17 и 18 веков. Гидроксид калия можно использовать для очистки изделий и поверхностей из нержавеющей стали при высоких температурах.
Вскоре после этого, в конце 19 века, едкий калий приобрел значение эмульгатора и регулятора кислотности, когда пищевая промышленность все больше использовала достижения химии для улучшения свойств продуктов. В настоящее время он используется для
- для создания и поддержания нужного уровня рН в шоколаде и продуктах на основе какао;
- для предохранения от потемнения, сохранения цвета и товарного вида замороженных овощей, особенно картофеля (как компонент обработки);
- для снятия шкурки и кожицы с овощей и фруктов;
- для проведения реакций рафинирования растительных масел (подсолнечного, льняного) в качестве катализатора.
Анизотропное травление кремния в кристаллах и для поглощения кислых газов, таких как сероводород и диоксид серы. Гидроксид калия можно использовать для дезинфекции сточных вод.
E525 очень широко используется в ветеринарии благодаря своей способности уничтожать клопов, блох, паразитов и некоторые вирусы и бактерии. Он содержится в дополнительном детском питании для детей в возрасте до одного года.

Это вещество также используется в других отраслях промышленности, процессах и материалах.
- алкалиновых батареях;
- моющих средствах;
- красителях;
- удобрениях;
- фармацевтике
- при получении вискозных нитей и волокон для обработки древесной целлюлозы;
- для обработки хлопковых тканей с целью придания им гигроскопичности.
Что такое калия гидроксид. Применение
Гидроксид калия является практически универсальным химическим соединением. Ниже приведены примеры материалов и процессы в которых он используется:
- .
В пищевой промышленности обозначается как пищевая добавка E525 . Используется как регулятор кислотности, в качестве осушителя и средства для снятия кожицы с овощей, корнеплодов и фруктов. Он также используется в качестве катализатора в некоторых реакциях.
Также используется для получения метана , поглощения кислотных газов и обнаружения некоторых катионов в растворах.
Популярное средство в производстве косметической продукции, вступая в реакцию с жирными маслами расщепляется и омыливает при этом масла.
В циркониевом производстве используется для получения обесфторенного гидроксида циркония .
В сфере промышленной мойки продукты на основе гидроксида калия, нагретые до 50-60 °С, применяются для очистки изделий из нержавеющей стали от жира и других масляных веществ, а также остатков механической обработки.
Используется в качестве электролита в щелочных (алкалиновых) батарейках .
Также применяется в ресомации — альтернативном способе «захоронения» тел.
Реакции править
Основность, растворимость и обезвоживающие свойства править
Вместо 100 г / 100 мл для NAOH, примерно 121 г KOH растворяется в 100 мл воды при комнатной температуре. Поэтому на молекулярной основе NaOH немного более растворим, чем KOH. Низкомолекулярные спирты, такие как метанол, этанол и пропанол, также являются отличными растворителями. Они участвуют в кислотно-щелочном балансе. В случае метанола образуется метоксид калия (метиловая соль):13
Из-за большого сродства к воде KOH может выступать в качестве лабораторного осушителя. Его часто используют для сушки основных растворителей, особенно аминов и пиридинов.
Как нуклеофил в органической химии править
Как и Наох, Кох является источником ОЗ. Это очень ядерный анион, который разрушает полярные связи как в минеральных, так и в органических материалах. Водные эфиры koh relaxes:.
Если R — длинная цепь, продукт называется калиевым мылом. Эта реакция проявляется в «маслянистом» ощущении при прикосновении — жир в коже быстро преобразуется в мыло и глицерин.
Расплавленный KOH используется вместо галогенидов и других выходных групп. Эта реакция особенно полезна для ароматических реагентов с образованием соответствующего фенола. 14
Реакции с неорганическими соединениями править
В дополнение к своей реактивности по отношению к кислотам, КОН разрушает оксиды
Поэтому важно отметить, что SiO2 атакуется КОН с образованием растворимого силиката калия. КОН реагирует с углекислым газом с образованием бикарбонатов
Получение.
В промышленном масштабе гидроксид калия получают электролизом хлористого калия. Возможны три варианта проведения электролиза: электролиз с твердым асбестовым или полимерным катодом (диафрагменный и мембранный методы производства), электролиз с жидким ртутным катодом (ртутный метод производства). В ряду электрохимических методов производства самым легким и удобным способом является электролиз с ртутным катодом, но этот метод наносит значительный вред окружающей среде в результате испарения и утечек металлической ртути. Мембранный метод производства самый эффективный, но и самый сложный. В то время как диафрагменный и ртутный методы были известны соответственно с 1885 и 1892 гг., мембранный метод появился сравнительно недавно – в 1970 гг.
Основной тенденцией в мировом производстве гидроксида калия в последние 10 лет является переход производителей на мембранный метод электролиза. Ртутный электролиз является устаревшей, экономически невыгодной и негативно действующей на окружающую среду технологией. Мембранный электролиз полностью исключает применение ртути. Экологическая безопасность мембранного метода заключается в том, что сточные воды после очистки вновь подаются в технологический цикл, а не сбрасываются в канализацию. При использовании данного метода решаются следующие задачи: исключается стадия сжижения и испарения хлора, водород используется для технологического пара, исключаются газовые выбросы хлора и его соединений. Мировым лидером в области мембранных технологий является японская компания «Асахи Касэй».
В России производство гидроксида калия осуществляется ртутным (ЗП КЧХК) и диафрагменным (Сода-Хлорат) методами.
Особенностью технологического оформления производства гидроксида калия является тот факт, что на аналогичных установках электролиза можно выпускать как едкий калий, так и каустическую соду. Это позволяет производителям без существенных капиталовложений переходить на производство гидроксида калия взамен каустической соды, производство которой не столь рентабельно, а сбыт в последние годы усложняется. При этом в случае изменений на рынке возможен безболезненный перевод электролизеров на производство ранее выпускавшегося продукта.
Примером перевода части мощностей с производства гидроксида натрия на гидроксид калия может служить ОАО «Завод полимеров КЧХК», начавший промышленный выпуск едкого кали на пяти электролизерах в 2007 году.
ОПРЕДЕЛЕНИЕ
Гидроксид калия (едкое кали)
представляет собой твердое вещество белого цвета (рис. 1). Весьма гигроскопичный, плавится и кипит без разложения.
Хорошо растворяется в воде с сильным экзо-эффектом, создает сильнощелочную среду.
Рис. 1. Гидроксид калия. Внешний вид.
Основные характеристики гидроксида калия приведены в таблице ниже:
Вред гидроксида калия
Работая на производстве с добавкой Е525 нельзя забывать о том, что это все-таки щелочь, которая относится ко второму классу опасности. Гидроокись калия может разъедать кожу и слизистые, вызывая химические ожоги. Избыток гидроксида калия, то есть длительный контакт с веществом провоцирует появление хронических кожных заболеваний.
На производстве, применяющем гидроксид калия, должны быть предприняты серьезные меры предосторожности. Особенно опасен контакт щелочи с глазами человека – зафиксированы случаи полной потери зрения
Гидроксид калия ещё называют едкое кали, поташ каустический, гидрат окиси калия, гидроокись калия, а ещё калиевая щелочь. По латыни название KOH звучит как Potassium hydroxide. Своими внешними данными и это вещество представляет кристаллы без цвета с высокой степенью гигроскопичности. В водных растворах КОН проявляет сильную щелочную реакцию. Путём проведения реакции диафрагменного электролиза раствора хлористого калия производят его получение. Гидроксид калия, благодаря своим уникальным свойствам, нашёл широкое применение в самых различных сферах жизнедеятельности человека.
В продажу КОН поступает в форме массивных блоков, вещества, подобного хлопьям, а также в виде гранул, некрупных кусков или 40-50% растворов. Из-за повышенной стоимости, химические соединения, имеющие в своём составе калий, не так распространены, как натриесодержащие. Ценовой вопрос стал причиной того, что они применяются в случаях, когда потребность в физико-химических свойствах не обеспечивают натриесодержащие вещества.
Являясь полностью безопасным, негорючим и абсолютно устойчивым к легкому воспламенению, гидроксид калия по воздействию на человеческий организм относится к соединениям второго класса. Опасность вызывает попадание едкого вещества на слизистые оболочки и даже на кожные покровы человека. Это может привести к тяжёлым и хроническим заболеваниям кожи. Особую опасность вызывает попадание вещества в глаза.
Промышленная фасовка раствора гидроксид калия происходит путём разлива в стальные бочки или специальные контейнеры по 100, 200 или 275 литров. В твёрдом виде для гидрата окиси калия используют чистые сухие барабаны на 50-180 дм. кубических. Для продукта чешуйчатого вида допускается использование ёмкостей с полиэтиленовыми вкладышами, равно как и мешки из полиэтилена.
В российской химической промышленности технический гидроксид калия удовлетворяет требованиям ГОСТа 9285-78, для химически чистого продукта предусмотрен ГОСТ 24363-80. Из-за границы сырьё КОН поступает в строгом соответствии стандарту CAS 1310-58-3.
Химическая реакция нейтрализации, в которой реагируют серная кислота, гидроксид калия с получением соли и воды известна всем со школьной скамьи. Но существуют и другие уникальные свойства КОН, которые нашли для этого вещества широкую область применения. Его используют, кроме как для нейтрализации кислот, ещё и в алкалиновых батареях, при катализе, производстве моющих средств, буровых растворов, красителей, удобрений.
Без использования гидроксид калия уже не обходится ни пищепром, ни газоочистка, ни металлургия, ни нефтеперегонка, ни фармацевтика. Его используют в производстве самых различных органических и неорганических веществ, бумаги, пестицидов, карбоната калия, калийных соединений, мыла, синтетического каучука.
Одной из важнейших сфер использования гидроксида калия является изготовление мягкого мыла. Моющие средства, шампуни, кремы для бритья, отбеливатели получают с использованием КОН
Другой важной областью применения этого вещества является получение востребованного промышленностью набора
В производстве перманганата калия заложен процесс сплавления каустического поташа с диоксидом марганца и последующее окисление полученного манганата калия в камере осуществления электролиза. Для получения можно использовать способ, аналогичный описанному выше. Но чаще его изготовляют путём сплавливания тонко молотой хромитной руды с гидроксидом (альтернатива — карбонат) калия, с последующим воздействием кислотой на полученный хромат.
Используя КОН с каустической содой можно добиться существенных результатов при производстве широкого спектра красителей, а также набора органических соединений. Он прекрасно проявляет себя как адсорбент газов, агент для дегидратации, вещество провоцирующее выпадение нерастворимых гидроксидов, электролит в типа.
И это только краткий перечень описания технологических процессов, в которых используется КОН.
Может ли добавка Е525 нанести вред здоровью человека
Однозначно на сегодняшний день известно только то, что вещество не приносит никакой пользы организму. В составе пищи количество щёлочной добавки настолько незначительно, что фактически никакой опасности она не представляет.
Для работы с калиевым щёлоком необходимо придерживаться техники безопасности: обязательно наличие защитной спецодежды, перчаток, маски, очков и специальной обуви.
Исследования, проведённые с использованием лабораторных животных показали, что постоянное употребление регулятора кислотности Е525 может стать причиной появления хронических заболеваний кожных покровов. Однако до сих пор нет установленной суточной нормы потребления добавки.
Вещество разрешено к использованию в процессе изготовления пищевых продуктов в России, Украине, Канаде, США и государствах Европейского союза. Сама по себе гидроокись калия представляет собой сильную щёлочь, поэтому при непосредственном контакте с чистой формой вещества человеку грозит опасность получения сильных ожогов и даже слепоты. В продуктах питания количество добавки настолько незначительно, что не причиняет здоровью вреда, более того, её разрешено использовать и в детском питании. Кроме изготовления еды, сфера использования гидроксида калия очень широка: это и производство различных моющих средств, химикатов, удобрений, бумаги, каучука, и перегонка нефти, и множество химических реакций разнообразного назначения, а также металлургические и буровые процессы.
Гидроксид калия – это щелочь, которую в пищевой промышленности называют добавкой Е525.
Другие часто встречающиеся названия гидроксида калия – это гидроокись калия, каустический поташ, калиевый щелок, едкое кали, potassium hydrate, сaustic potash, potassium hydroxide.
Применение гидроксида калия в качестве пищевой добавки разрешено в странах ЕС, в России, Украине.
Гидроксид калия
Если не указано иное, данные приведены для материалов при нормальных условиях (25°C 77°C, 100 кПа).
Гидроксид калия — это неорганическое соединение с типом K OH, которое обычно называют едким кали.
Наряду с гидроксидом натрия (NAOH), это бесцветное твердое вещество является оригинальным сильным основанием. Он имеет множество промышленных и профессиональных применений, большинство из них — кислотно-едкие и реактивные. По оценкам, в 2005 году было произведено от 700 000 до 800 000 тонн. KOH, как и многие другие калийсодержащие химикаты, является предшественником большинства мягких и жидких мыл. Это белое твердое вещество, которое вызывает опасную эрозию. В большинстве коммерческих образцов она составляет около. 90% чистоты, остальное — вода и карбонат. 10
Получение
Также при решении задач возникают вопросы про способы получения вещества – предпочтительно знать лабораторный вариант и промышленный, который активно применяется на территории страны.
Получение в лаборатории
В условиях лаборатории гидроксид получается посредством проведения простой химической реакции – раствор просто пропускается через анионит (также допускается использование раствора поташа и известковой воды для получения тех же результатов от проведенного действия). Остается отделить образовавшийся нерастворимый осадок удобным способом, а оставшаяся жидкость и будет гидроксидом калия.
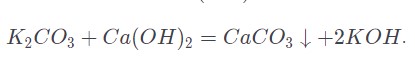
Получение в промышленности
Промышленный способ приготовления гидролиза водного раствора хлорида калия или же карбоната калия при использовании железного катода.
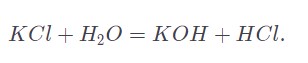
В промышленном направлении может использоваться поташа и известковой воды.
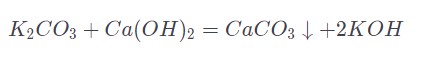
Области применения гидроксида калия
Едкое кали – одна из наиболее распространенных щелочей, которая благодаря своим свойствам активно применяется в различных сферах и областях промышленности, в строительстве и бытовых нуждах:
- В качестве пищевой добавки гидроксид калия (Е525) используется как регулятор кислотности. Эту щелочь применяют в изготовлении какао, шоколада и продукции, их содержащей;
- Производство мыла и шампуней, отбеливателей и средств для бритья, а также другой бытовой химии происходит с применением гидроксида калия;
- Химическая промышленность с помощью каустического поташа получает метан и использует едкое кали для обнаружения в растворах катионов и поглощения кислотных газов;
- В промышленной мойке очищение изделий из нержавеющей стали от жира происходит с помощью нагретых до 50-60°С растворов, содержащих гидроксид калия;
- Едкое кали служит электролитом в щелочных батарейках;
- В строительстве применяется для изготовления таких материалов, как штукатурка, гипсовые растворы, побелка;
-
Гидроксид калия способен очищать сточные воды от взвешенных и коллоидных частиц
; - В производстве металлов используется для нейтрализации отработанных вредных газов;
- В медицине едкое кали может применяться для лечения кислотных ожогов, а также для дезинфекции корневых зубных каналов в стоматологии;
- В целлюлозно-бумажной промышленности используется для предотвращения образования пены во время производства бумаги и картона.
- Гидроксид калия добавляют в морскую воду с целью сокращения объема углекислого газа в атмосфере и смягчения парникового эффекта;
- Едкое кали используется в борьбе с клещами, блохами и другими насекомыми;
- Создание очагов заземления для электротехники также происходит с участием этого вещества, так как это соединение способно значительно снижать удельное сопротивление грунта;
-
Жители Афганистана используют гидроксид калия для производства табака и в качестве краски для своих домов
.
Афганистан, Швеция, Норвегия, Индия и Пакистан – наиболее крупные потребители едкого кали. Несмотря на пользу, которую может принести его использование, избыток гидроксида калия, то есть слишком большая его доля в растворах и составах, может нанести непоправимый ущерб как материалу, с которым производится работа, так и здоровью человека, применяющего щелочь.
Гидроксид калия удобрение. Использование гидроокиси калия
 Современные интенсивные технологии возделывания сельскохозяйственных культур предусматривают использование большого количества удобрений и химических средств, достигая определенного повышения продуктивности, но это удается сделать ценой все большего загрязнения почвы и окружающей среды.
Современные интенсивные технологии возделывания сельскохозяйственных культур предусматривают использование большого количества удобрений и химических средств, достигая определенного повышения продуктивности, но это удается сделать ценой все большего загрязнения почвы и окружающей среды.
Поэтому все технологии возделывания сельскохозяйственных культур должны базироваться на всемерном поддержании гомеостаза растений, на помощь растительному организму реализовать его наследственно обусловленную программу воспроизводства потомства на повышение урожайности и направлена на оптимизацию режима питания растений.
95% сухого вещества формируется растением в процессе фотосинтеза и системы питания предполагают значительное снижение применения минеральных удобрений. Идея снижения норм минеральных удобрений особенно актуальной стала в последнее время в связи с ухудшением экологической ситуации.
Целесообразнее провести смещение реакции среды в листьях – в период старения, а в потребляющих органах – с начала их формирования. Для этого предложен новый способ регулирования жизнедеятельности растений, усиления перемещения пластических веществ по растению путем использования простых неорганических веществ и соединений, которые исключают загрязнение окружающей среды: гидроокись калия (для повышения аттрагирующей способности акцепторов) и уксусную кислоту (для повышения донорской функции листьев).
После применения этих веществ урожайность зерновых и зернобобовых культур повышается на 15%. На посевах сахарной свеклы сахаристость корнеплодов повышается на 1,2% в результате применения уксусной кислоты.
Реакции с гидроксидом калия
Щелочной калий легко реагирует с кислотными оксидами. В конце процесса образуются умеренно или кислотные соли. Конечный продукт зависит от соотношения реагентов. Например, если преобладает гидроксид калия: реакция протекает следующим образом.
Если преобладает монооксид углерода: уравнение выглядит следующим образом
Кроме того, гидроксид калия легко реагирует как с амфотерными оксидами, так и с гидроксидами. Конечными продуктами реакции являются соли — умеренные и сложные:.
Щелочной калий также реагирует с солями кислот с образованием менее кислых промежуточных солей.
Этот химикат вступает в реакцию с простыми веществами. Исключение составляют инертные газы азот, кислород, водород и углерод, выделяющий водород.
При добавлении щелочи происходит реакция окисления с выделением кислорода.
Вещество реагирует с серой только при повышении температуры. При нормальных условиях вещества не реагируют друг с другом.
Вещество вступает в реакцию с растворимыми солями. Например, осадки хлорида калия и гидроксида меди образуются при добавлении хлорида меди к щелочи.
Вред пищевого эмульгатора Е525 Гидроксид калия
Стоит отметить, что гигроскопичность пищевого эмульгатора Е525 Гидроксид калия значительно отличается по силе от другого схожего по строению вещества гидроксида натрия. Хотя добавка и отнесена к веществам, разрешенным к применению в производственных процессах пищевой отрасли существует вред пищевого эмульгатора Е525 Гидроксид калия для человеческого организма. Как правило, вред пищевой эмульгатор Е525 Гидроксид калия может нанести при попадании концентрированного химического соединения на слизистые или кожные покровы человека.
Наиболее активно пищевой эмульгатор Е525 Гидроксид калия используют в составе таких продуктов питания как: какао, а также большинство производных продуктов питания, изготовленных на основе какао-масла или порошка, кроме того замороженные овощи или фрукты, детские продукты питания. Пищевой эмульгатор Е525 Гидроксид калия имеет широкий спектр применения, который не ограничивается интересами исключительно пищевой промышленности. К примеру, гидроксид калия используют для синтезирования метана.
Пищевой эмульгатор Е525 Гидроксид калия способен распознать в составе всевозможных растворов катионы, т.е. ионы, которые несут положительный или плюсовой электрический заряд. При воздействии на пищевой эмульгатор Е525 Гидроксид калия высокими температурами соединение начинает проявлять свойства, которые используют для очистки изделий из нержавеющих материалов от различных загрязнений, к примеру масла или других жиросодержащих веществ.
Специалисты предостерегают от негативных последствий воздействия пищевого эмульгатора Е525 Гидроксид калия на человека и говорят о необходимости соблюдения повышенных мер безопасности при работе с небезопасным соединением. Считается, что наибольшие повреждения и тяжелый вред пищевой эмульгатор Е525 Гидроксид калия может нанести при попадании соединения в глаза. Гидроксид калия запросто разрушает более прочные материалы, чем слизистые и кожные покровы человеческого тела. По данной причине следует избегать прямого контакта с пищевым эмульгатором Е525 Гидроксид калия.
-
Повреждения груди. Разрыв диафрагмы.
-
Диета Американские горки (Диета Мартина Катана) — меню, отзывы, результаты, советы
-
Противовоспалительная терапия. Элиминационная терапия.
-
Оциллококцинум при беременности: инструкция по применению в 1, 2 и 3 триместрах — как принимать, особенности на ранних сроках
- Варенье из малины: польза и вред, рецепты
Применение гидроксида калия
Если брать во внимание исключительно пищевую промышленность, то здесь, чаще всего, Е525 используют производители шоколада, какао и продукции из них. Помимо этого, гидроксид калия может встречаться в составе продуктов детского питания, им обрабатывают замороженный картофель
Помимо этого, гидроксид калия может встречаться в составе продуктов детского питания, им обрабатывают замороженный картофель.
Калиевый щелок могут использовать в качестве вспомогательного средства на производстве овощной и фруктовой продукции – при помощи вещества очищают фрукты, овощи и корнеплоды.
В косметической промышленности гидроксид калия применяют для производства шампуней, мыла, отбеливателей, средств для бритья.
Где взять гидроксид калия. Как получить гидроксида натрия и гидроксида калия
Получение NaOH (Гидроксид натрия) и KOH (Гидроксид Калия).
Опишу, как получить NaOH из Na2CO3 (Кальцинировання сода). Для калияаналогично, только вместо соды взять поташ (весовые доли будут другие).
Общие сведения.NaOH – едкий натрий. Входит в состав чистящего средства «Крот».Применяется при изготовлении хлората калия методом электролиза,глицерина, а также некоторых ВВ. Других его применений в пиротехнике я, ксожалению не знаю. На его основе можно попробовать сделать манганатнатрия, который может заменять марганцовку в некоторых составах(например, с магнием). Лично я манганат натрия (Na2MnO4) не делал, нодумаю, что он имеет схожие с манганатом калия свойства, который здоровожахнул в смеси с магнием.
Реактивы:
1) Сода стиральная (Na2CO3) . 2) Са(OH)2 – гашеная известь (лучше купить так называемую бордосскую смесь (медный купорос + Ca(OH)2)). Продается в садоводческих магазинах.
Оборудование:
Изготовление.
1. Отвесите 10гр Соды и 7гр Гашеной извести.
2. Растворите Соду в воде и подогрейте сосуд, чтобы вся сода растворилась.
3. Добавьте гашеную известь.Na2CO3 + Ca(OH)2 → CaCO3↓ + 2NaOH
4. Отфильтруйте осадок (обычный мел) и выпарите раствор.
5. Полученную гадость растолките в ступке.
Внимание!Едкое вещество! Работайте только в перчатках!
Свойства
У любого химического элемента есть свойства, на основании которых определяется направление его применения и особенности получения. Знание всех свойств элементов имеет значение в решении задач, которые попадаются при прохождении школьного курса химии и экзаменационных задачах.
Физические свойства
Гидроксид напоминает массу гигроскопического типа, имеет белый характерный окрас. Молярная масса составляет 56,11 грамм на моль, а плотность при средней температуре в 25 градусов составляет 2,004 грамма на кубический сантиметр.
Показатели плавления установлены на уровне 405 градусов и, чтобы вскипятить соединение, придется осуществить его нагревание до 1325 градусов. Кипение сопровождается реакцией.
Химические свойства
Способен диссоциировать на катионы калия и анионы гидроксогруппы.
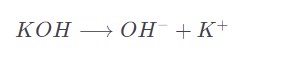
В данном случае такое сочетание относится к щелочным, то есть активно вступает в хим. реакции.
Щелочи при взаимодействии с сильными кислотами нейтрализуются, то есть раствор получается нейтральным. При нейтрализации образуется вода и средняя соль.
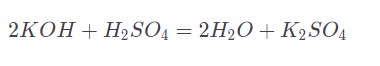
Гидроксид вступает в реакции обмена, из-за которых производится образование осадков или оксидов.
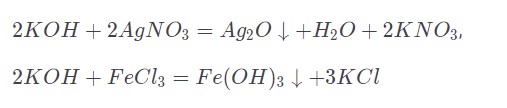
При воздействии повышенных температур гидроксид способен вступать в реакции с активными металлами (бериллий, алюминий, цинк, олово, свинец и сурьма), а также с оксидными и гидроксидными соединения от них с образованием соли, а также выделением газа или образованием воды.
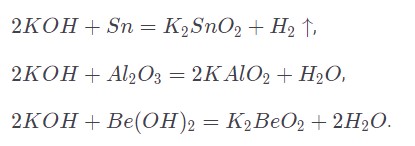
В водной среде образуются гидроксокомплексы.
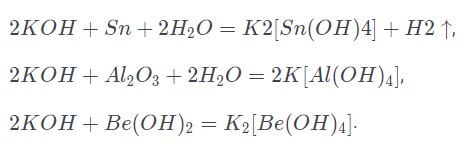
Водный раствор способен вступать в реакцию с бором, кремнием и германием, а также их оксидами и кислотами.
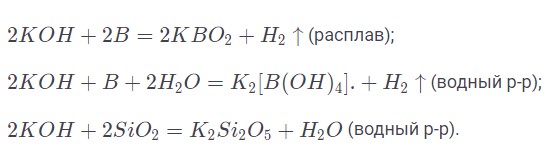
Реакции с сернистым и углекислым газом протекают без доп. факторов с образованием гидросоединений.
Реакция с диоксидом азота предполагает получение нитрита и нитрата.
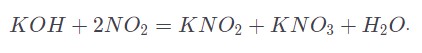
При протекании реакции с угарным газом образуется формиат калия.
Для определения наличия ионов калия в составе того ли иного химического соединения изучим процесс его горения – калий дает фиолетовую окраску пламени. Если в составе вещества также имеются ионы натрия – необходимо будет рассматривать результат при использовании синего светофильтра.
Гидроксид калия уравнение. Al(OH)3 + KOH = ? уравнение реакции
Закончите уравнение реакции Al(OH)3 + KOH = ? Расставьте стехиометрические коэффициенты. Запишите молекулярное уравнение реакции. Охарактеризуйте соединение гидроксид алюминия: приведите его основные физические и химические свойства. Каким образом его можно получить в лаборатории? А в промышленности?
1 ответ
В результате взаимодействия гидроксида калия с гидроксидом алюминия, проявляющим амфотерные свойства, из-за чего эта реакция и становится возможной (Al(OH)3 + KOH = ?) может происходить образование разных продуктов. Так, если реакцию проводили в концентрированном растворе гидроксида калия , то получается комплексная соль тетрагидроксоалюминат калия; в случае же разбавленного раствора щелочи образуется двойная соль алюминат калия и вода (обмен). Молекулярные уравнения реакции имеют вид:
Запишем ионные уравнения, учитывая, что вода и гидроксид алюминия на ионы не распадаются, т.е. не диссоциируют.
Первое уравнение называют полным ионным, а второе – сокращенным ионным. Гидроксид алюминия представляет собой термически неустойчивый порошок белого цвета. Не растворяется в воде. Он существует в виде четырех полиморфных модификаций, каждую из которых можно выделить при конкретной температуре.Гидроксид алюминия выпадает в виде студенистого осадка при действии щелочей на растворы солей алюминия и легко образует коллоидные растворы.
Гидроксид алюминия – типичный амфотерный гидроксид. С кислотами он образует соли, содержащие катион алюминия, со щелочами – алюминаты; при взаимодействии с водными растворами щелочей образуются гидроксоалюминаты; при нагревании до температуры вышегидроксид алюминия разлагается.
Свойства гидроксида калия
Едкое кали обладает следующими свойствами:
- Гигроскопичность – способность поглощать водяные пары, именно этим обусловлено свойство гидроксида калия расплываться на открытом воздухе. Хранить каустический поташ необходимо в плотно закрытой упаковке в сухом помещении;
- Способность растворяться в метиловом и этиловом спирте при 28°С и в воде уже при 0°С с выделением большого количества тепла;
- Едкое кали получило свое название благодаря свойству разрушать многие органические материалы (бумагу, кожу, древесину и т.д.);
-
Гидроксид калия не обладает горючестью, но взрывоопасен
.
Эти свойства каустического поташа делают работу с ним довольно опасной, но, с другой стороны, значительно расширяют сферы применения данного вещества.





























